新冠小分子原創(chuàng)新藥FB2001研發(fā)階段中期項目可行性研究報告
思瀚產(chǎn)業(yè)研究院 2022-05-05
本次投資項目包括公司新冠小分子原創(chuàng)新藥 FB2001 研發(fā)階段中的 I 期臨床試驗�,全球 II/III 期臨床試驗(截至中期分析階段)�,以及質(zhì)量與工藝研究���。
(一)項目背景
1、醫(yī)藥行業(yè)規(guī)模增長迅速���,市場前景廣闊
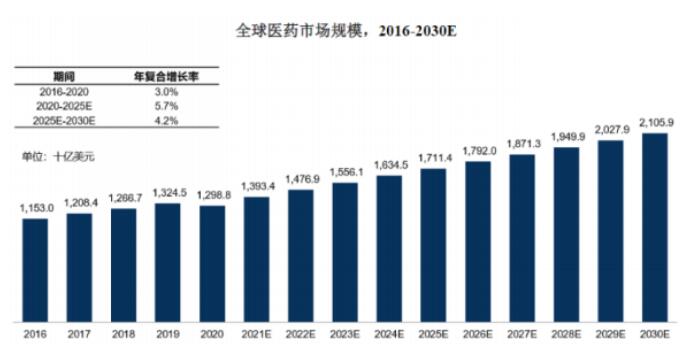
隨著人口老齡化趨勢加劇���、社會醫(yī)療衛(wèi)生支出持續(xù)增加以及醫(yī)藥研發(fā)投入的不斷增長,全球醫(yī)藥產(chǎn)業(yè)的市場規(guī)模穩(wěn)定增長。根據(jù) Frost&Sullivan 數(shù)據(jù)����,2020年全球醫(yī)藥市場規(guī)模已達到 12,988 億美元����,預計到 2025 年��,全球醫(yī)藥市場規(guī)模將達到 17,114 億美元�����,2020 年至 2025 年的復合年增長率為 5.7%����。預計到 2030年�,全球醫(yī)藥市場規(guī)模將達到 21,059 億美元,2025 年至 2030 年的復合年增長率為 4.2%。
數(shù)據(jù)來源:Frost & Sullivan
隨著經(jīng)濟和醫(yī)療需求的增長�����,中國醫(yī)藥市場保持著穩(wěn)定增長��。根據(jù) Frost &Sullivan 數(shù)據(jù),2016 年中國醫(yī)藥市場規(guī)模達到約 13,294 億人民幣,并在接下來以2.2%的復合年增長率增長至 2020 年的 14,480 億元�����。預計未來 5 年�,中國醫(yī)藥市場將會以 9.6%的復合年增長率于 2025 年達到 22,873 億元���,并于 2030 年達到29,911 億元�����。行業(yè)規(guī)模增長迅速�����,市場前景廣闊���。
數(shù)據(jù)來源:Frost & Sullivan 思瀚整理
2����、政策鼓勵和促進國產(chǎn)創(chuàng)新藥發(fā)展
隨著中國醫(yī)療衛(wèi)生體制改革的深入,國家藥品集采和藥價談判��、一致性評價�����、藥品上市許可持有人制度�����、醫(yī)保嚴格控費����、新藥降價加速納入醫(yī)保��、新藥評審加速等政策陸續(xù)推出�����,我國創(chuàng)新藥的研發(fā)環(huán)境迎來重大變化�,醫(yī)藥行業(yè)面臨洗牌����,具有真正創(chuàng)新能力和核心競爭力的創(chuàng)新藥企�����,特別是擁有領(lǐng)先技術(shù)能力和成本優(yōu)勢的醫(yī)藥企業(yè)迎來了發(fā)展機遇���。從 2017 年開始,國家藥監(jiān)局加速新藥審評審批�����,帶動中國創(chuàng)新藥企業(yè)發(fā)展�,并且��,國家通過醫(yī)保談判讓更多創(chuàng)新藥可以更快的納入醫(yī)保支付范圍�����,為創(chuàng)新藥研發(fā)提供了較好的發(fā)展環(huán)境�����。
3、全球范圍疫情反復,亟需更多新冠小分子治療藥物
(1)全球疫情反復,新的病毒株帶來多輪新增高峰
根據(jù)美國約翰霍普金斯大學發(fā)布的統(tǒng)計數(shù)據(jù)顯示,截至 2022 年 3 月,全球新冠肺炎確診病例總數(shù)超過 4.60 億例���,全球累計死亡病例超過 607 萬例��,死亡率約 1.3%����。
新冠病毒自 2020 年 1 月起,就從原始毒株不斷演化分支出多個變異毒株種類,截至 2022 年3 月,新冠病毒株已迭代了超過 14 種分型,包括阿爾法(B.1.1.7���,2020 年 9 月出現(xiàn)于英國)�、貝塔(B.1.351���,2020 年 5 月出現(xiàn)于南非)����、伽馬(P.1��,2020 年 11 月出現(xiàn)于巴西)、德爾塔(B.1.617.2�����,2020 年 10 月出現(xiàn)于印度)和奧密克戎(B.1.1.529,2021 年 11 月出現(xiàn)于南非)����。
根據(jù) Nextstrain 統(tǒng)計數(shù)據(jù)�����,2022 年開始,奧密克戎及其變異毒株 BA.2 成為新冠肺炎患者中的主流變異株,而同時在中國大陸��,自奧密克戎于 2022 年 1 月9 日在天津檢出后����,后續(xù)又在河南、遼寧、廣東、上海和北京等多地出現(xiàn)����,引發(fā)了多輪的感染人數(shù)劇增����,成為新一輪的防控焦點�。
資料來源:Nextstrain 思瀚整理
奧密克戎及其變種具有高傳染性����,所帶來的患者數(shù)量的增加給全球衛(wèi)生體系造成了巨大壓力。根據(jù)美國 CDC 數(shù)據(jù)���,即使奧密克戎導致的死亡率顯著低于德爾塔�����,仍在短期內(nèi)帶來了住院及死亡人數(shù)的上升,在 2021 年 12 月至 2022 年 3月奧密克戎流行期間���,美國住院病人數(shù)為 1,165,483 人�����,死亡人數(shù)為 194,685 人�����。奧密克戎流行期間與德爾塔流行期間的住院人數(shù)及死亡人數(shù)���,沒有顯著差異�。
注 1:2020 年度住院率數(shù)據(jù)時間段為 2020 年 8 月-2020 年 12 月���。
資料來源:美國 CDC��,https://covid.cdc.gov/covid-data-tracker/#new-hospital-admissions綜上,新冠病毒株的變異具有不確定性,新的變異毒株在全球范圍造成了多輪疫情爆發(fā)�,并在短期內(nèi)帶來新冠肺炎住院患者人數(shù)及死亡人數(shù)的上升。全球醫(yī)療資源面臨極大壓力,全球范圍內(nèi)對新冠治療藥品需求持續(xù)旺盛�����。
(2)我國將長期面臨境外輸入壓力��,需要新冠小分子藥物應(yīng)對風險
截至 2022 年 4 月 20 日,全國 31 個省(自治區(qū)�����、直轄市)累計確診病例超過 19 萬人,共造成約 4,655 人死亡��,2022 年以來��,受奧密克戎毒株境外輸入影響����,疫情在我國香港���、廣東����、上海�、吉林等地散點式爆發(fā)�����,疫情存在數(shù)輪反復。
數(shù)據(jù)來源:國家衛(wèi)健委����,31 個?���。ㄗ灾螀^(qū)�、直轄市)數(shù)據(jù)不包括港澳臺地區(qū)
新冠肺炎爆發(fā)以來��,我國始終堅持“動態(tài)清零”的方針����,因長期面臨境外輸入壓力�����,新冠疫情在局部地區(qū)反復�,因此國內(nèi)需要新冠治療藥物來控制新冠肺炎散點式爆發(fā)帶來的風險����。
(3)老齡����、基礎(chǔ)疾病����、低免疫力及未接種疫苗人群,或?qū)㈤L期面臨較高風險
全球新冠肺炎住院患者中��,老齡�����、患有基礎(chǔ)疾病、低免疫力及未接種疫苗人群在新冠肺炎疫情中的中重癥及死亡率遠超其他年齡段人口��。
根據(jù)美國 CDC 數(shù)據(jù)�����,在美國接近 100 萬的新冠肺炎死亡病例中,65 歲以上老人占到近 68 萬例�,以 18-29 歲人群感染新冠病毒后的住院和死亡風險為基線來比較�����,50-64 歲人群的住院風險提高了 4 倍�����、死亡風險提高了 30 倍�;65-74 歲人群的住院風險提高了 5 倍���、死亡風險提高了 90 倍����;75-84 歲人群的住院風險提高了 9 倍��、死亡風險提高了 220 倍;85 歲以上人群的住院風險提高了 15 倍��、死亡風險提高了 570 倍。
數(shù)據(jù)來源:美國 CDC���,數(shù)據(jù)截至 2022 年 2 月 12 日
同時�,基于美國 CDC 截至 2021 年 12 月 31 日的統(tǒng)計數(shù)據(jù)��,美國新冠住院患者中(按美國新冠治療方案�,住院患者主要為中��、重癥患者)��,多數(shù)患者患有高血壓(56%)、代謝疾?�。?1%)及心血管疾?。?7%)等基礎(chǔ)疾病��,表明患有基礎(chǔ)疾病的人群面臨較高的風險�����。
美國住院患者中基礎(chǔ)性疾病人群占比(單位:%)
數(shù)據(jù)來源:美國 CDC,數(shù)據(jù)截至 2021 年 12 月 31 日
根據(jù)香港衛(wèi)生署數(shù)據(jù),2021 年 12 月 31 日至 2022 年 4 月 17 日���,香港新增新冠感染者 1,185,807 例,累計住院患者 49,149 人����,住院率 4.14%����,主要集中在3 歲以下嬰幼兒及 60 歲以上老齡人口��,其中 80 歲及以上人群的中重癥比例最高。
數(shù)據(jù)來源:香港衛(wèi)生署�����,https://www.coronavirus.gov.hk/sim/index.html
同時�����,60 歲以上老齡人群由于免疫能力較低、普遍患有基礎(chǔ)疾病以及疫苗接種率較低(香港 60 歲及以上人群的 2 劑及以上疫苗接種率僅為 49%��,遠低于30-59 歲年齡組 80%的接種率,80 歲及以上年齡組的 2 劑及以上疫苗接種率僅為18%)���,住院率及死亡率顯著高于青壯年人群��。
數(shù)據(jù)來源:香港衛(wèi)生署
此外,根據(jù)倫敦國王學院及蓋伊和圣托馬斯國家醫(yī)療服務(wù)體系基金會的一項研究發(fā)現(xiàn),免疫系統(tǒng)較弱的患者特別容易長期感染新冠病毒,且長期感染可能是新的新冠變種的來源,其中一名患者感染新冠長達 505 天�����,體內(nèi)攜帶了包括阿爾法����、伽馬和奧密克戎在內(nèi)的 10 種突變���。在此背景下,低免疫力患者需要長期接受抗病毒治療,新冠小分子治療藥物將滿足該類群體的長期抗病毒需求�����。
(4)全球存在大量風險人群�,新冠小分子藥物對住院患者具有長期價值在全球疫情環(huán)境下,老齡、患有基礎(chǔ)疾病、低免疫力及未接種疫苗人群�����,或?qū)㈤L期面臨較高風險��。
數(shù)據(jù)表明����,全球存在大量高齡�����、患有基礎(chǔ)疾病����、低免疫力及未接種疫苗的高風險人群,且部分人群數(shù)量仍將處于上升趨勢�。由于新冠病毒會較長期流行并且發(fā)生變異�,因此新冠疫情帶來的重癥和死亡病例將持續(xù)出現(xiàn)�����,抗病毒藥物不僅具有短期防疫價值,也是中長期抗擊疫情的必備武器���,具有長期戰(zhàn)略價值。
(5)國家鼓勵新冠病毒特效藥物研發(fā)及產(chǎn)業(yè)化發(fā)展
在新冠疫情背景下���,國家出臺多項政策鼓勵新冠病毒特效藥物研發(fā)及產(chǎn)業(yè)化���。2022 年 2 月�����,國家藥監(jiān)局藥審中心發(fā)布《新型冠狀病毒肺炎抗病毒新藥臨床試驗技術(shù)指導原則(試行)》���,針對新冠藥物的研發(fā)以及上市標準制定了一系列指導原則���,鼓勵申請人與審評機構(gòu)進行溝通交流�。2022 年 3 月�,第十三屆全國人民代表大會第五次會議批準的《關(guān)于 2021 年國民經(jīng)濟和社會發(fā)展計劃執(zhí)行情況與 2022 年國民經(jīng)濟和社會發(fā)展計劃草案的報告》中強調(diào)“根據(jù)疫情防控需要進一步加快新冠病毒藥物國內(nèi)研發(fā)上市”����。同時����,全國多地發(fā)布了助力新冠藥品研發(fā)上市的政策措施���,支持新冠小分子治療藥物加快科技研發(fā)和產(chǎn)業(yè)化�。
2022 年 3 月 14 日����,國家衛(wèi)健委發(fā)布《新型冠狀病毒肺炎診療方案(試行第九版)》,首次將輝瑞 Paxlovid 納入診療方案�,用于輕型和普通型且伴有進展危重型高風險因素的患者,此為我國診療方案中首次添加新冠小分子藥物��。疫情防治方案的調(diào)整將指引藥物研發(fā)的新方向�,加速我國新冠小分子藥物的研發(fā)及產(chǎn)業(yè)化進程。
4��、本次發(fā)行符合公司發(fā)展戰(zhàn)略要求
公司致力于成為具有國際領(lǐng)先水平的創(chuàng)新型生物醫(yī)藥公司�,研發(fā)、生產(chǎn)����、銷售中國自主研發(fā)的原創(chuàng)新藥��,打造全球知名的中國創(chuàng)新藥品牌��。
公司專注抗病毒領(lǐng)域的藥物研究開發(fā)十余年�,由 DONGXIE(謝東)博士領(lǐng)導的創(chuàng)始人團隊擁有豐富的抗病毒領(lǐng)域創(chuàng)新藥開發(fā)經(jīng)驗和專業(yè)知識����,公司創(chuàng)始人團隊平均擁有二十年以上豐富的行業(yè)經(jīng)驗���。
公司始終保持對人才的高度重視����,結(jié)合公司未來的研發(fā)規(guī)劃布局�,加快人才引進步伐,開展多元化的人才儲備��。藥物研發(fā)涉及多學科交叉合作�,公司研發(fā)人員結(jié)構(gòu)科學合理,專業(yè)背景涉及醫(yī)學�、藥學、化學����、生物學等專業(yè)領(lǐng)域�����。從業(yè)經(jīng)歷能夠覆蓋藥物分子設(shè)計和發(fā)現(xiàn)��、臨床方案的設(shè)計與實施�、法規(guī)市場藥品的注冊與獲批����、生產(chǎn)工藝放大與質(zhì)量管控等研發(fā)核心環(huán)節(jié)。
此外�,公司經(jīng)過十余年的積累,與傳染病治療領(lǐng)域知名醫(yī)療機構(gòu)以及業(yè)內(nèi)頂尖臨床專家開展了廣泛�、緊密的臨床試驗合作,得到業(yè)內(nèi)機構(gòu)和專家的高度認可�,為公司研發(fā)管線中其他產(chǎn)品的臨床試驗順利實施打下良好的基礎(chǔ)。
本次向特定對象發(fā)行股票所涉及的募投項目有助于加快公司臨床研究工作及推動相關(guān)產(chǎn)品在國內(nèi)外的上市進程�����,推動新冠小分子藥物成為公司第二款實現(xiàn)全球商業(yè)化的產(chǎn)品��,有利于公司核心發(fā)展戰(zhàn)略的實現(xiàn)和生產(chǎn)經(jīng)營的持續(xù)健康發(fā)展�。
(二)項目建設(shè)的必要性
1、推動公司新冠小分子藥物研發(fā)����,滿足全球市場需求�����,助力抗擊疫情
(1)全球新冠疫情或?qū)㈤L期持續(xù)��,小分子藥物為新冠治療提供有效救治
在全球疫情反復的背景下�����,新冠藥物需求日益增加。根據(jù)美國約翰霍普金斯大學發(fā)布的統(tǒng)計數(shù)據(jù)顯示����,截至 2022 年 3 月,全球新冠肺炎確診病例總數(shù)超過4.60 億例����,全球累計死亡病例超過 607 萬例。
在全球多國放寬疫情管控�、病毒不斷變異、部分疫苗對變異毒株保護效力降低���、新冠特效治療藥物需求尚未被完全滿足的背景下����,全球新冠疫情可能長期持續(xù),抗病毒藥物將為疫苗接種后的突破性感染以及未接種疫苗的感染者提供有效救治��。
(2)公司新冠小分子藥物 FB2001���,技術(shù)路徑優(yōu)異��,試驗數(shù)據(jù)顯示對主要變異毒株均有效
公司在研產(chǎn)品 FB2001�,為注射用新冠肺炎病毒(SARS-CoV-2)蛋白酶抑制劑�����,擬用于治療新冠肺炎住院患者���。公司擁有FB2001在全球范圍內(nèi)的臨床開發(fā)�、生產(chǎn)���、制造及商業(yè)化權(quán)利��。
FB2001 具有明確的藥物作用機制:蛋白酶抑制劑�����,靶向 3CL 蛋白酶���。3CL蛋白酶(又稱主蛋白酶 Mpro)是一種半胱氨酸蛋白酶�����,是在冠狀病毒中發(fā)現(xiàn)的主要蛋白酶��,參與病毒中 pp1a 和 pp1ab 蛋白切割��,成為成熟的 16 種非結(jié)構(gòu)蛋白�,這些非結(jié)構(gòu)蛋白參與亞基因組 RNA 的合成�����,在病毒生命周期中發(fā)揮重要作用�����。3CL 蛋白酶抑制劑通過與 3CL 蛋白酶結(jié)合���,使其無法再正常結(jié)合底物,從而抑制病毒復制,3CL 蛋白酶序列高度保守����,其抑制劑在臨床前研究中可展現(xiàn)出對包括奧密克戎在內(nèi)的 SARS-CoV-2 主要變異毒株的抑制活性;同時�,由于 3CL蛋白酶沒有人類同源物,安全性良好�。
FB2001 具有廣譜抗病毒活性:研究顯示,F(xiàn)B2001 對主要流行的 SARS-CoV-2 變異病毒株阿爾法����、貝塔、德爾塔�����、奧密克戎均具有高效廣譜抑制活性���。FB2001對新冠肺炎病毒 3CL 蛋白酶的抑制活性 IC??為 0.053 ±0.005μM����,上述研究成果已發(fā)表于國際權(quán)威期刊《科學》(Science)并作為封面文章刊登��。
FB2001 無需聯(lián)用藥代激動劑:研究顯示��,F(xiàn)B2001 單藥在人體的藥物濃度已達到預測的有效劑量,無需聯(lián)合藥代動力學增強劑(如利托那韋等)����,可以減少因使用藥代動力學增強劑出現(xiàn)的潛在藥物相互作用風險,從而滿足新冠肺炎住院患者對安全性高����、藥物相互作用小的抗新冠病毒藥物的需求。
綜上����,公司在研產(chǎn)品注射用 FB2001 技術(shù)路徑優(yōu)異、安全性好��,截至目前的研究試驗數(shù)據(jù)顯示�,F(xiàn)B2001 對主要流行的新冠變異病毒株均有效。
(3)公司產(chǎn)品 FB2001 是國內(nèi)開發(fā)進度最快的 3CL 蛋白酶抑制劑��,符合我國抗新冠小分子藥物自主可控的戰(zhàn)略方向
全球已上市的新冠小分子藥物均表現(xiàn)出相對顯著的治療作用���,國內(nèi)也有多家藥企布局新冠小分子藥物的開發(fā),處于不同的臨床開發(fā)階段���。
截至本預案披露日�,國家藥品監(jiān)督管理局藥品審評中心(CDE)已同意公司開展 FB2001 有效性和安全性的國際多中心、隨機�、雙盲、安慰劑對照的 II/III 期臨床研究�����,F(xiàn)B2001 美國 I 期臨床即將完成最后一個劑量組的研究���。
截至本預案披露日��,公司 FB2001 研發(fā)進度在已知 3CL 蛋白酶抑制劑中進度位于國內(nèi)第一�、全球前列�,有望成為我國首個 3CL 蛋白酶抑制劑,符合我國新冠小分子藥物國產(chǎn)自主可控的國家戰(zhàn)略��。全球主要的 3CL 蛋白酶抑制劑如下:
(4)全球 3CL 蛋白酶抑制劑開發(fā)主要針對輕�、中癥門診患者,公司產(chǎn)品FB2001 將填補全球住院人群治療市場的空白
目前已上市的新冠小分子治療藥物�,如輝瑞 Paxlovid、默沙東 Molnupiravir等�,均適用于輕、中癥患者���,僅吉利德 Remdesivir(瑞德西韋)適應(yīng)癥范圍包括 住院患者���,全球范圍內(nèi)尚無針對新冠住院患者的 3CL 蛋白酶抑制劑藥物����,存在 較大的市場空白��。
根據(jù)吉利德財報�����,2021 年瑞德西韋實現(xiàn)銷售收入 55.65 億美元��,同比增長98%�,已在全球累計治療超過 1,000 萬患者,在美國有超過 50%的新冠肺炎住院 患者使用瑞德西韋進行治療�。
2021 年 12 月至今,奧密克戎毒株已成為全球范圍內(nèi)的主要流行毒株�����,根據(jù)吉利德財報�,2022 年第一季度瑞德西韋實現(xiàn)銷售收入 15.35 億美元,同比增長 5%��。作為目前上市產(chǎn)品中唯一用于住院患者的抗新冠病毒小分子藥物���,瑞德西韋 龐大及快速增長的產(chǎn)品收入規(guī)模代表了全球新冠肺炎住院患者治療領(lǐng)域���,具有可 觀的市場規(guī)模及增長空間。
公司注射用 FB2001 擬適用人群為全球新冠住院患者�,這類患者主要包括高齡、患有基礎(chǔ)疾病�、低免疫力及未接種疫苗的高風險人群,該類群體在新冠疫情下面臨的風險遠高于青壯年群體��,并且大多都有進行相關(guān)疾病的藥物治療���。
綜上����,本次募集資金將進一步推動公司新冠小分子藥物研發(fā)����,助力抗擊疫情,填補全球市場空白�,推進我國新冠小分子藥物自主可控。
2��、增強公司創(chuàng)新藥物研發(fā)能力�,增強公司核心競爭力
研發(fā)是創(chuàng)新藥企業(yè)的發(fā)展基石和核心競爭力���。醫(yī)藥行業(yè)屬技術(shù)密集型產(chǎn)業(yè),產(chǎn)品生命周期有限��,技術(shù)迭代升級較快����,創(chuàng)新藥企業(yè)為保持競爭優(yōu)勢,不斷儲備拓展研發(fā)管線產(chǎn)品��,增強研發(fā)的深度和廣度��,為持續(xù)增長����、增強核心競爭力提供保障。全球醫(yī)藥行業(yè)的龍頭企業(yè)持續(xù)進行大量的研發(fā)投入以進行創(chuàng)新產(chǎn)品的開發(fā)���,從而保持行業(yè)領(lǐng)導地位和產(chǎn)品體系的競爭力���,創(chuàng)造新的增長點。我國醫(yī)藥行業(yè)近年來研發(fā)投入力度不斷加大�����,傳統(tǒng)制藥企業(yè)和創(chuàng)新藥物企業(yè)紛紛開展了一系列接軌國際技術(shù)水平的創(chuàng)新藥物研發(fā),帶動行業(yè)技術(shù)水平整體快速發(fā)展�����。
在這一趨勢當中����,公司必須不斷加大技術(shù)投入����,才能保障公司適應(yīng)境內(nèi)外醫(yī)藥行業(yè)的技術(shù)發(fā)展特征,鞏固產(chǎn)品的市場地位���,增強公司核心競爭力���。通過本次募投項目的實施,將加快公司新冠小分子原創(chuàng)新藥的研發(fā)進程��,拓展公司在研藥物的臨床試驗廣度和深度�����,為公司實現(xiàn)更多可商業(yè)化的產(chǎn)品奠定基礎(chǔ)�����。
3、股權(quán)融資是適合公司抓住機遇快速發(fā)展的融資方式
股權(quán)融資能使公司保持良好的資本結(jié)構(gòu)�����,使公司擁有足夠的長期資金����,降低經(jīng)營風險和財務(wù)風險,有利于公司利用自身優(yōu)勢不斷提高綜合競爭力����,鞏固并提升行業(yè)地位和盈利能力。
(三)項目建設(shè)的可行性
1���、政策可行性為本項目的實施提供了有利因素
近年來我國政府部門出臺了一系列政策�,扶持和鼓勵醫(yī)藥行業(yè)開展創(chuàng)新藥品的研發(fā)和產(chǎn)業(yè)化��?���!蛾P(guān)于藥品注冊審評審批若干政策的公告》、《藥品上市許可持有人制度試點方案》、《“十三五”國家戰(zhàn)略新興產(chǎn)業(yè)規(guī)劃》����、《關(guān)于深化審評審批制度改革鼓勵藥品醫(yī)療器械創(chuàng)新的意見》、《關(guān)于鼓勵藥品創(chuàng)新實行優(yōu)先審評審批的意見》等政策中����,都對具有明顯臨床價值、技術(shù)水平和國際接軌的創(chuàng)
新藥物的產(chǎn)業(yè)化提出了鼓勵和扶持���。縮短創(chuàng)新藥物臨床申請和上市申請的審批時間���,加快有潛力的新藥進入市場�,滿足臨床上的迫切需求�。創(chuàng)新藥的專利保護也大大加強。此外�,政府還出臺了人才激勵計劃和專項公共研發(fā)基金等優(yōu)惠政策,特別是支持國內(nèi)企業(yè)的研發(fā)活動���。
同時����,在新冠疫情背景下,國家出臺多項政策鼓勵新冠病毒特效藥物研發(fā)及產(chǎn)業(yè)化���。2022 年 2 月��,國家藥監(jiān)局藥審中心發(fā)布《新型冠狀病毒肺炎抗病毒新藥臨床試驗技術(shù)指導原則(試行)》�����,針對新冠藥物的研發(fā)以及上市標準制定了一系列指導原則�,鼓勵申請人與審評機構(gòu)進行溝通交流�����。2022 年 3 月�����,第十三屆全國人民代表大會第五次會議批準的《關(guān)于 2021 年國民經(jīng)濟和社會發(fā)展計劃執(zhí)行情況與 2022 年國民經(jīng)濟和社會發(fā)展計劃草案的報告》中強調(diào)“根據(jù)疫情防控需要進一步加快新冠病毒藥物國內(nèi)研發(fā)上市”���。同時����,全國多地發(fā)布了助力新冠藥品研發(fā)上市的政策措施���,支持新冠小分子治療藥物加快科技研發(fā)和產(chǎn)業(yè)化���。
因此�����,國家產(chǎn)業(yè)政策的有力支持�����,為本項目的實施創(chuàng)造了良好的外部條件�。
2��、技術(shù)可行性為本項目的開展奠定了基礎(chǔ)保障
基于自主創(chuàng)新����,公司擁有多項處于國際或國內(nèi)先進水平的核心技術(shù)���,并已全面應(yīng)用在各主要產(chǎn)品的研發(fā)設(shè)計當中�,實現(xiàn)了科技成果的有效轉(zhuǎn)化���。整體來看��,公司已擁有自主研發(fā)的技術(shù)創(chuàng)新平臺���,形成了豐富的產(chǎn)品儲備���,積累了大量新藥開發(fā)的經(jīng)驗,能夠高效的推進在研產(chǎn)品的臨床進展��。公司現(xiàn)有的創(chuàng)新藥物的發(fā)現(xiàn)和在全球范圍內(nèi)的臨床研究和開發(fā)的能力共同為本項目提供充分的技術(shù)可行性���。
3�����、優(yōu)秀的研發(fā)團隊為本項目的進行提供了人才可行性
公司組建了素養(yǎng)扎實����、經(jīng)驗豐富���、結(jié)構(gòu)完整的研發(fā)團隊����,團隊成員來自全球知名研究機構(gòu)����、領(lǐng)先的國際制藥公司以及 FDA 等監(jiān)管機構(gòu)成員�����,通過過往的工作經(jīng)歷以及公司自主研發(fā)過程中累計的經(jīng)驗���,使得公司形成未來可復制的創(chuàng)新藥研發(fā)綜合實力,包括藥物分子設(shè)計和發(fā)現(xiàn)���、臨床方案的設(shè)計與實施�、法規(guī)市場藥品的注冊與獲批�����、生產(chǎn)工藝放大與質(zhì)量管控等各個核心環(huán)節(jié)����,成為公司不斷衍生并拓展產(chǎn)品管線的原動力�。
公司研發(fā)團隊技術(shù)知識結(jié)構(gòu)合理,專業(yè)領(lǐng)域涵蓋新藥研發(fā)的各個方面���,包括藥學��、制藥工程��、生物制藥���、分析化學�����、藥物制劑����、微生物學等學科專業(yè)背景為本項目的實施提供了充分的人才可行性����。同時,F(xiàn)B2001 項目攻關(guān)團隊還包括中國科學院上海藥物研究所和中國科學院武漢病毒研究所�,在藥物設(shè)計、藥化和機制研究����,多種給藥路徑藥效評價方面具有世界領(lǐng)先水平的技術(shù)支撐。
(四)投資概算
本次募集資金投資項目計劃投資總額為 35,307 萬元��,其中��,擬投入募集資金 30,000 萬元,其余以自籌資金投入�,投資明細如下:
其中,臨床研究費用主要包括臨床試驗費用��、臨床樣品生產(chǎn)費用����、質(zhì)量研究費用、注冊費用����、臨床人員工資等;質(zhì)量與工藝研究費用主要包括用于原料藥與制劑工藝質(zhì)量與工藝研究費用�����;引進授權(quán)費用主要公司向合作方支付的開發(fā)里程碑款項���。
(五)實施主體�����、項目整體進度安排
1、實施主體
本項目實施主體為前沿生物藥業(yè)(南京)股份有限公司及其全資子公司�����。
2、項目整體進度安排
本次募集資金投資項目包括公司新冠小分子原創(chuàng)新藥 FB2001 研發(fā)階段中的 I 期臨床試驗�,全球 II/III 期臨床試驗(截至中期分析階段),以及質(zhì)量與工藝研究��。公司將根據(jù)項目實施情況���,有序推進研發(fā)進度�����。
(六)項目備案情況
截止本預案公告日��,公司尚未完成項目立項備案���,相關(guān)程序的辦理不存在實質(zhì)性障礙。
(七)項目效益分析
本項目的實施�,將公司加快在研新藥研發(fā)進程,推動在研產(chǎn)品的盡快上市����。由于藥品需要完成臨床試驗、獲得新藥注冊批件和生產(chǎn)文號后再進行商業(yè)化���,還涉及產(chǎn)品生產(chǎn)�����、銷售推廣等多個領(lǐng)域�����,因此本募投項目無法單獨直接計算經(jīng)濟效益�。
此報告為正式可研報告摘取部分,個性化定制請咨詢思瀚產(chǎn)業(yè)研究院�����。
免責聲明:
1.本站部分文章為轉(zhuǎn)載�����,其目的在于傳播更多信息��,我們不對其準確性��、完整性��、及時性、有效性和適用性等任何的陳述和保證�����。本文僅代表作者本人觀點����,并不代表本網(wǎng)贊同其觀點和對其真實性負責����。
2.思瀚研究院一貫高度重視知識產(chǎn)權(quán)保護并遵守中國各項知識產(chǎn)權(quán)法律。如涉及文章內(nèi)容����、版權(quán)等問題,我們將及時溝通與處理��。








 美國亞利桑那州-記憶綿床墊生產(chǎn)基地擴建項目可行性研究報告
美國亞利桑那州-記憶綿床墊生產(chǎn)基地擴建項目可行性研究報告 江西宜春-高能量密度動力儲能(方形)鋰電池研發(fā)產(chǎn)業(yè)化項目可行性研究報告
江西宜春-高能量密度動力儲能(方形)鋰電池研發(fā)產(chǎn)業(yè)化項目可行性研究報告 水晶光電-臺州智能終端用光學組件技改項目可行性研究報告
水晶光電-臺州智能終端用光學組件技改項目可行性研究報告 廣西欽州-中偉股份北部灣產(chǎn)業(yè)基地三元項目一期可行性研究報告
廣西欽州-中偉股份北部灣產(chǎn)業(yè)基地三元項目一期可行性研究報告 中國天津-毫米波雷達研發(fā)中心建設(shè)項目可行性研究報告
中國天津-毫米波雷達研發(fā)中心建設(shè)項目可行性研究報告 中國重慶-國儲珞璜智慧物流園項目可行性研究報告
中國重慶-國儲珞璜智慧物流園項目可行性研究報告 安徽合肥-高性能微電子級聚酰亞胺膜材料項目可行性研究報告
安徽合肥-高性能微電子級聚酰亞胺膜材料項目可行性研究報告 廣東汕頭-生殖健康藥品整體升級項目可行性研究報告
廣東汕頭-生殖健康藥品整體升級項目可行性研究報告