西安市高新區(qū)-肝靶向抗乙肝��、肝癌等新藥研發(fā)項(xiàng)目可行性研究報(bào)告
思瀚產(chǎn)業(yè)研究院 新通藥物 2023-01-06
1����、項(xiàng)目情況
本項(xiàng)目將用于五個(gè)在研藥物:肝靶向抗乙肝藥物甲磺酸帕拉德福韋(Pradefovir)����、肝靶向抗肝癌藥物 MB07133、潛在長(zhǎng)效性肝靶向抗乙肝藥物富馬酸海普諾福韋(HTS)�����、治療全身性強(qiáng)直-陣攣性癲癇持續(xù)狀態(tài)���,預(yù)防和治療神經(jīng)外科圍手術(shù)期和手術(shù)中引起的癲癇發(fā)作用藥的 CE-磷苯妥英鈉注射液、HBV 核衣殼蛋白裝配抑制劑的研發(fā)費(fèi)用�����,包括臨床前研究費(fèi)用�����、臨床試驗(yàn)費(fèi)用�、人工費(fèi)用以及注冊(cè)費(fèi)用等��,從而推動(dòng)產(chǎn)品的研發(fā)進(jìn)展以及上市進(jìn)度���。
項(xiàng)目實(shí)施地點(diǎn)為西安市高新區(qū)錦業(yè)路 69 號(hào) C 區(qū) 12 號(hào)。項(xiàng)目實(shí)施主體為西安新通藥物研究股份有限公司�����。
2��、項(xiàng)目的必要性
(1)加快公司創(chuàng)新藥物研發(fā)進(jìn)程��,滿足更廣闊的市場(chǎng)和患者需求
我國(guó)是乙肝大國(guó)�,乙肝的治療是影響民生領(lǐng)域的大問(wèn)題。據(jù)《慢性乙型肝炎防治指南(2019 年版)》�����,全球約有 2.57 億乙肝病毒感染者����,每年約有 88.7 萬(wàn)人死于感染相關(guān)疾病,世界一半的乙肝患者在中國(guó)�。
肝癌為中國(guó)第四大頻發(fā)的癌癥,且致死率在所有癌癥中排名第二。根據(jù)弗若斯特沙利文統(tǒng)計(jì)��,2020 年���,中國(guó)有超過(guò) 37.9 萬(wàn)肝癌新發(fā)患者��,其五年存活率僅為 12.1%����,遠(yuǎn)低于中國(guó)癌癥整體存活率 40.5%��,主要原因是其致病的復(fù)雜性和藥物作用靶點(diǎn)暫不明確�����,目前缺少有效的治療手段��,未滿足的臨床需求將成為肝癌藥物市場(chǎng)發(fā)展的主要驅(qū)動(dòng)力����。
根據(jù)弗若斯特沙利文統(tǒng)計(jì)����,2016 年,中國(guó)癲癇持續(xù)狀態(tài)患者為 54.4 萬(wàn)人,2020 年增長(zhǎng)至 75.3 萬(wàn)人�����,年復(fù)合增長(zhǎng)率 8.5%��;預(yù)計(jì) 2024 年患者將突破 100 萬(wàn)人�����。此外��,癲癇是神經(jīng)外科手術(shù)后常見的伴隨癥狀�����。2020 年中國(guó)腦外科手術(shù)接受預(yù)防癲癇治療的患者人數(shù)為 68.7 萬(wàn)�����,年復(fù)合增長(zhǎng)率 14.4%����。目前國(guó)內(nèi)尚無(wú)專門針對(duì)手術(shù)預(yù)防癲癇的藥品獲批,該產(chǎn)品是說(shuō)明書上唯一批準(zhǔn)的神經(jīng)外科手術(shù)預(yù)防用藥��。
自 2011 年開始,公司依托授權(quán)引進(jìn)及自主研發(fā)的藥物專利技術(shù)�,開發(fā)布局針對(duì)上述治療領(lǐng)域的在研藥物。截至報(bào)告簽署日����,公司主要在研管線共有 9 條,涵蓋乙肝�、肝癌、癲癇等重大疾病領(lǐng)域����。
未來(lái)三年,公司將繼續(xù)圍繞長(zhǎng)期發(fā)展戰(zhàn)略規(guī)劃�,加速產(chǎn)品臨床開發(fā)和產(chǎn)業(yè)化的進(jìn)程,包括 CE-磷苯妥英鈉注射液��、甲磺酸帕拉德福韋�����、注射用 MB07133���、富馬酸海普諾福韋片和 HBV 核衣殼蛋白裝配抑制劑等,推進(jìn)更多臨床前候選化合物進(jìn)入全球臨床試驗(yàn)���,持續(xù)豐富公司產(chǎn)品管線�����。因此�,公司需要通過(guò)市場(chǎng)化融資推進(jìn)在研藥物的研發(fā)、臨床及產(chǎn)業(yè)化等進(jìn)程��。
(2)增強(qiáng)研發(fā)實(shí)力�����,鞏固公司行業(yè)地位和競(jìng)爭(zhēng)優(yōu)勢(shì)
發(fā)行人是一家專注藥物研發(fā)超過(guò)二十年的高新技術(shù)企業(yè)���,現(xiàn)聚焦于乙肝�����、肝癌等重大疾病領(lǐng)域���,致力于研發(fā)具有自主知識(shí)產(chǎn)權(quán)、安全有效���、以臨床價(jià)值為導(dǎo)向的創(chuàng)新藥物�����,同時(shí)引進(jìn)并開發(fā)一款國(guó)內(nèi)臨床未滿足需求的癲癇藥物����。經(jīng)過(guò)多年的研發(fā)積累,目前已經(jīng)建立了完整的新藥研發(fā)體系��,形成了創(chuàng)新藥物研發(fā)的核心技術(shù)���。
醫(yī)藥行業(yè)屬于技術(shù)密集型產(chǎn)業(yè)�����,技術(shù)迭代升級(jí)較快�����,創(chuàng)新藥企業(yè)為保持競(jìng)爭(zhēng)優(yōu)勢(shì)��,不斷儲(chǔ)備拓展研發(fā)管線�����,增強(qiáng)研發(fā)的深度和廣度��。公司“新藥研發(fā)項(xiàng)目”的順利實(shí)施�,將有利于公司增強(qiáng)研發(fā)實(shí)力�,進(jìn)一步完善和開發(fā)核心技術(shù),從而鞏固公司行業(yè)地位和產(chǎn)品體系的競(jìng)爭(zhēng)力��。
3����、項(xiàng)目的可行性
(1)國(guó)家政策對(duì)創(chuàng)新藥的支持
在國(guó)家鼓勵(lì)創(chuàng)新的大背景下,近年來(lái)有關(guān)方面出臺(tái)一系列政策大力支持醫(yī)藥企業(yè)創(chuàng)新��。2017 年 10 月��,中共中央辦公廳和國(guó)務(wù)院辦公廳發(fā)布了《關(guān)于深化審評(píng)審批制度改革鼓勵(lì)藥品醫(yī)療器械創(chuàng)新的意見》�,從改革臨床試驗(yàn)管理、加快上市審評(píng)審批���、促進(jìn)藥品創(chuàng)新等多方面支持創(chuàng)新�����;2018 年 11 月��,CDE 發(fā)布了《關(guān)于優(yōu)化優(yōu)先審評(píng)申請(qǐng)審核工作程序的通知》���,進(jìn)一步細(xì)化了政策的落地����,相關(guān)政策鼓勵(lì)國(guó)內(nèi)醫(yī)藥企業(yè)創(chuàng)新的同時(shí)����,也對(duì)國(guó)際醫(yī)藥公司創(chuàng)新藥上市簡(jiǎn)化了行政審批;2019 年《中華人民共和國(guó)藥品管理法》與 2020 年《藥品注冊(cè)管理辦法》的出臺(tái)�����,讓我國(guó)在藥品審批制度上與國(guó)際接軌�����,符合條件的藥物可通過(guò)突破性治療藥物����、附條件批準(zhǔn)、優(yōu)先審評(píng)審批���、特別審批四個(gè)加快通道獲批上市���。國(guó)家藥監(jiān)局不斷加大改革力度�,加速創(chuàng)新藥的審批流程��,提升了患者的藥物可及性及治療方式�。
(2)公司具備較強(qiáng)的研發(fā)實(shí)力��、自主創(chuàng)新能力和成果轉(zhuǎn)化能力
發(fā)行人是一家專注藥物研發(fā)超過(guò)二十年的高新技術(shù)企業(yè)��,能在高風(fēng)險(xiǎn)的新藥研發(fā)領(lǐng)域找準(zhǔn)藥品研發(fā)方向�,累計(jì)取得臨床批件、新藥證書和生產(chǎn)批件百余件���,累計(jì)簽訂技術(shù)轉(zhuǎn)讓合同金額 7.6 億元���,形成了成熟的成果轉(zhuǎn)化和商業(yè)化能力。
截至本報(bào)告簽署日�,公司累計(jì)承擔(dān)科研項(xiàng)目 36 項(xiàng),其中國(guó)家重大新藥創(chuàng)制項(xiàng)目 7 項(xiàng)�����、國(guó)家級(jí)中小型企業(yè)創(chuàng)新基金 2 項(xiàng)�����、省部級(jí)課題 21 項(xiàng)、市級(jí)課題 6 項(xiàng)���。公司兩個(gè) 1 類新藥甲磺酸帕拉德福韋和注射用 MB07133 被連續(xù)列入“十二五”���、“十三五”國(guó)家重大新藥創(chuàng)制計(jì)劃。
目前�����,公司擁有肝靶向創(chuàng)新藥物研發(fā)平臺(tái)和多項(xiàng)專利技術(shù)�,形成 8 個(gè)主要在研產(chǎn)品,其中 1 個(gè)產(chǎn)品已經(jīng)提交上市許可申請(qǐng)��、1 個(gè)產(chǎn)品已完成 III 期臨床試驗(yàn)的核心臨床階段并提交 Pre-NDA 會(huì)議溝通申請(qǐng)�����、1 個(gè)產(chǎn)品處于 II 期臨床試驗(yàn)第二階段����、1 個(gè)產(chǎn)品處于 Ic/IIb 期臨床試驗(yàn)階段,1 個(gè)產(chǎn)品已獲準(zhǔn)開展臨床試驗(yàn)���。
綜上�,公司擁有核心創(chuàng)新研發(fā)平臺(tái)以及自主研發(fā)能力,形成了豐富的產(chǎn)品儲(chǔ)備����;具備創(chuàng)新藥開發(fā)能力和經(jīng)驗(yàn),能夠高效推進(jìn)在研產(chǎn)品的臨床進(jìn)展�����,實(shí)現(xiàn)創(chuàng)新藥物成果轉(zhuǎn)化�����,完成產(chǎn)業(yè)化和商業(yè)化進(jìn)程�����。公司的研發(fā)實(shí)力和自主創(chuàng)新能力為本項(xiàng)目提供了充分的技術(shù)可行性�����。
(3)公司擁有一線研發(fā)一流人才和長(zhǎng)期從事藥物研發(fā)的管理團(tuán)隊(duì)
公司的核心研發(fā)團(tuán)隊(duì)具有深厚的行業(yè)背景及豐富的新藥研發(fā)管理經(jīng)驗(yàn)��,始終堅(jiān)持以臨床價(jià)值為導(dǎo)向的創(chuàng)新驅(qū)動(dòng)理念����,在業(yè)內(nèi)享有被認(rèn)可的業(yè)績(jī)和超過(guò) 20 年的新藥研發(fā)及管理經(jīng)驗(yàn)。在創(chuàng)新藥的研發(fā)方面具有一線專業(yè)技術(shù)人員��、管理人員及專家顧問(wèn)團(tuán)隊(duì)��,具有臨床前研究�、中試生產(chǎn)、臨床研究�����、注冊(cè)申報(bào)����、臨床開發(fā)及產(chǎn)業(yè)化研究等完整的新藥研發(fā)成功經(jīng)驗(yàn)。
公司優(yōu)秀的研發(fā)人才以及經(jīng)驗(yàn)豐富的管理團(tuán)隊(duì)��,為本項(xiàng)目的實(shí)施提供了有利的保障���。
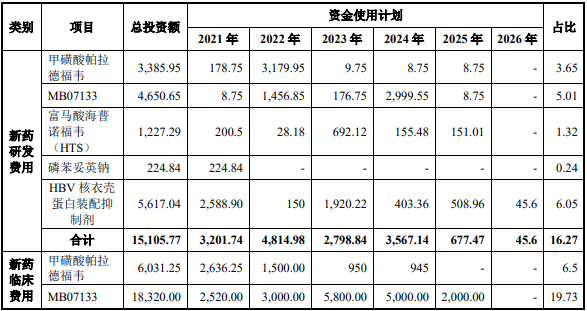
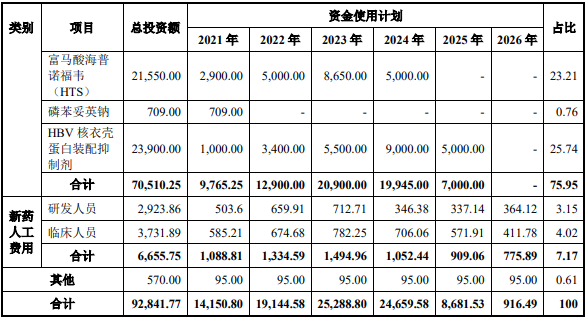
4�、項(xiàng)目具體投資內(nèi)容及投資進(jìn)度
本項(xiàng)目投資總額為 92,841.77 萬(wàn)元�,具體投資構(gòu)成情況如下表所示:?jiǎn)挝唬喝f(wàn)元,%
5��、各研發(fā)項(xiàng)目的市場(chǎng)情況
當(dāng)前乙肝治療藥物主要為核苷(酸)類藥物( NAs )和干擾素-α(包括Peg-IFNα),能夠有效抑制乙肝病毒增殖�,減緩乙肝患者的肝硬化進(jìn)程,但是無(wú)法治愈乙肝�����。根據(jù)弗若斯特沙利文分析�����,目前主流用藥是核苷(酸)類藥物��,約占乙肝用藥市場(chǎng)的 80%��,一線核苷(酸)類藥物是 TDF��、TAF 和 ETV���。
核苷(酸)類藥物長(zhǎng)期治療能顯著改善肝臟組織學(xué),顯著降低肝硬化并發(fā)癥和肝細(xì)胞癌的發(fā)生率���。鑒于核苷(酸)類藥物作為逆轉(zhuǎn)錄酶抑制劑�,可強(qiáng)效抑制乙肝病毒復(fù)制����,長(zhǎng)期治療能顯著改善肝臟組織學(xué)���,顯著降低肝硬化并發(fā)癥和肝細(xì)胞癌的發(fā)生率,但均不能直接抑制 cccDNA 的轉(zhuǎn)錄活性��,從而無(wú)法有效抑制病毒蛋白如表面抗原(HBsAg)的表達(dá)��,因此絕大多數(shù)患者需要長(zhǎng)期甚至終身服用���。當(dāng)前推薦的一線核苷(酸)類藥物均能長(zhǎng)期有效抑制病毒復(fù)制�,因此長(zhǎng)期用藥的安全性問(wèn)題越來(lái)越受到關(guān)注�����。
目前一系列針對(duì)乙肝病毒生命周期的各個(gè)關(guān)鍵步驟以及免疫相關(guān)宿主因子的候選治療藥物正在進(jìn)行或即將進(jìn)入臨床試驗(yàn)����,包括病毒進(jìn)入抑制劑、病毒轉(zhuǎn)錄抑制劑���、病毒聚合酶抑制劑�����,核衣殼組裝調(diào)節(jié)劑和 HBsAg 分泌抑制劑等��。借鑒丙肝藥物的成功經(jīng)驗(yàn)����,通過(guò)多途徑、多靶點(diǎn)�����、多藥物聯(lián)合阻斷 HBV 的生物學(xué)合成��,結(jié)合免疫治療將可能實(shí)現(xiàn)慢性乙肝的治愈����。
根據(jù)《原發(fā)性肝癌診療指南(2022 年版)》,對(duì)肝癌的臨床階段和治療方案的選擇取決于癌細(xì)胞的數(shù)量����、大小��、血管侵襲程度和肝外轉(zhuǎn)移程度��。
目前���,肝癌的治療方法主要可分為局部治療和系統(tǒng)治療�����。局部治療主要分為手術(shù)治療��、介入治療�、放療等。對(duì)于早期肝癌患者���,局部治療中的外科治療(包括手術(shù)切除與肝移植)是首選的治療方法和唯一能使患者獲得長(zhǎng)期生存乃至治愈的手段�。
在我國(guó)����,大多數(shù)肝癌患者確診時(shí)已經(jīng)達(dá)到中晚期,手術(shù)�、介入、放療等局部治療手段固然重要����,但是往往會(huì)復(fù)發(fā)轉(zhuǎn)移,難以滿足臨床治療的需求��,這就需要依靠全身性的系統(tǒng)治療���,即藥物治療來(lái)實(shí)現(xiàn)控制腫瘤��、提高患者的療效�����。
近年來(lái)���,以 PD-1/PD-L1 抗體為代表的腫瘤免疫療法興起����,PD-1/PD-L1 抗體在多個(gè)腫瘤中表現(xiàn)出出色療效��,已成為目前市場(chǎng)關(guān)注的熱點(diǎn)����。雖然在 PD-1 單抗單藥療效不明顯,但聯(lián)合用藥方案顯示出了較大的潛力�����。前述新興療法��,尤其是腫瘤免疫療法與小分子藥聯(lián)合療法的出現(xiàn)將帶來(lái)優(yōu)異的生存獲益�����,可能將目前肝細(xì)胞癌藥物療法平均數(shù)月的用藥時(shí)間大幅提高����,延長(zhǎng)患者的生存期和用藥時(shí)間。
目前癲癇的治療方法較多�,近年來(lái)在藥物治療、神經(jīng)調(diào)控等方面都有許多進(jìn)展��,現(xiàn)在常用治療的方法可以分為:藥物治療�、外科治療(包括神經(jīng)調(diào)控療法)、生酮飲食等�。當(dāng)一次癲癇發(fā)作(包括各種類型癲癇發(fā)作)持續(xù)時(shí)間大大超過(guò)了該型癲癇發(fā)作大多數(shù)患者發(fā)作的時(shí)間,或反復(fù)發(fā)作�,在發(fā)作間期患者的意識(shí)狀態(tài)不能恢復(fù)基線,被稱為癲癇持續(xù)狀態(tài)����。其中主要適應(yīng)于癲癇持續(xù)狀態(tài)藥物包括苯巴比妥類、苯二氮?類����、二苯并氮?類、丙戊酸鈉類藥物等。
對(duì)于神經(jīng)外科圍手術(shù)期或外傷后的患者�,術(shù)后應(yīng)及時(shí)給以靜脈或肌注抗癲癇藥物,以迅速達(dá)到有效血藥濃度����。但是國(guó)內(nèi)尚無(wú)專門針對(duì)手術(shù)預(yù)防癲癇的藥品獲批,現(xiàn)在主要的產(chǎn)品多為超適應(yīng)癥用藥�。苯妥英鈉是一種最常用、研究最多��、FDA推薦的預(yù)防性靜脈抗癲癇藥物���。但由于苯妥英鈉難溶于水����,且在水中易降解�����,不易制成注射液�,在我國(guó)苯妥英鈉注射液已停產(chǎn)。磷苯妥英鈉作為苯妥英鈉的磷酸酯前藥�,易溶于水,從而在保持與苯妥英鈉相同療效與安全性的前提下�,解決了苯妥英鈉難溶于水的難題����。磷苯妥英鈉注射液作為苯妥英鈉注射液改良產(chǎn)品����,于1996 年在美國(guó)上市����,但并未引入中國(guó)。
此報(bào)告為正式報(bào)告摘取部分�。需編制政府立項(xiàng)、銀行貸款���、投資決策等用途可行性研究報(bào)告咨詢思瀚產(chǎn)業(yè)研究院��。
免責(zé)聲明:
1.本站部分文章為轉(zhuǎn)載�,其目的在于傳播更多信息���,我們不對(duì)其準(zhǔn)確性��、完整性���、及時(shí)性����、有效性和適用性等任何的陳述和保證���。本文僅代表作者本人觀點(diǎn)�����,并不代表本網(wǎng)贊同其觀點(diǎn)和對(duì)其真實(shí)性負(fù)責(zé)��。
2.思瀚研究院一貫高度重視知識(shí)產(chǎn)權(quán)保護(hù)并遵守中國(guó)各項(xiàng)知識(shí)產(chǎn)權(quán)法律�。如涉及文章內(nèi)容�����、版權(quán)等問(wèn)題�����,我們將及時(shí)溝通與處理�����。









 美國(guó)亞利桑那州-記憶綿床墊生產(chǎn)基地?cái)U(kuò)建項(xiàng)目可行性研究報(bào)告
美國(guó)亞利桑那州-記憶綿床墊生產(chǎn)基地?cái)U(kuò)建項(xiàng)目可行性研究報(bào)告 江西宜春-高能量密度動(dòng)力儲(chǔ)能(方形)鋰電池研發(fā)產(chǎn)業(yè)化項(xiàng)目可行性研究報(bào)告
江西宜春-高能量密度動(dòng)力儲(chǔ)能(方形)鋰電池研發(fā)產(chǎn)業(yè)化項(xiàng)目可行性研究報(bào)告 水晶光電-臺(tái)州智能終端用光學(xué)組件技改項(xiàng)目可行性研究報(bào)告
水晶光電-臺(tái)州智能終端用光學(xué)組件技改項(xiàng)目可行性研究報(bào)告 廣西欽州-中偉股份北部灣產(chǎn)業(yè)基地三元項(xiàng)目一期可行性研究報(bào)告
廣西欽州-中偉股份北部灣產(chǎn)業(yè)基地三元項(xiàng)目一期可行性研究報(bào)告 中國(guó)天津-毫米波雷達(dá)研發(fā)中心建設(shè)項(xiàng)目可行性研究報(bào)告
中國(guó)天津-毫米波雷達(dá)研發(fā)中心建設(shè)項(xiàng)目可行性研究報(bào)告 中國(guó)重慶-國(guó)儲(chǔ)珞璜智慧物流園項(xiàng)目可行性研究報(bào)告
中國(guó)重慶-國(guó)儲(chǔ)珞璜智慧物流園項(xiàng)目可行性研究報(bào)告 安徽合肥-高性能微電子級(jí)聚酰亞胺膜材料項(xiàng)目可行性研究報(bào)告
安徽合肥-高性能微電子級(jí)聚酰亞胺膜材料項(xiàng)目可行性研究報(bào)告 廣東汕頭-生殖健康藥品整體升級(jí)項(xiàng)目可行性研究報(bào)告
廣東汕頭-生殖健康藥品整體升級(jí)項(xiàng)目可行性研究報(bào)告